体内CAR-T,走到爆发前夜
更新时间:
2025-08-09 19:53:21.132

这是同写意T20+大会的分会之一,一场关于体内CAR-T(in vivo CAR-T)的大讨论正引燃全场——眼前看到的这番水泄不通的景象,或许正是当下医药界“顶流”体内CAR-T热度的最生动注脚。
MNC早已嗅到风暴的气息。
从阿斯利康的10亿美元,到艾伯维的21亿美元,巨头接连掷下重注,不仅刷新生物技术领域并购规模纪录,更以真金白银为体内CAR-T的“溢价”能力背书,彻底点燃了这条赛道的熊熊火焰。
据不完全统计,全球有超过20款管线处于临床前或临床早期,Interius、Umoja、EsoBiotec处于第一梯队,国内包括济因生物、云顶新耀、合源生物、沙砾生物、易慕峰生物、博生吉医药等创新力量也加速布局。
两个月前,有企业创始人去新奥尔良参加美国细胞与基因治疗学会(ASGCT)年度会议,明显地察觉到,年会上涉及体内CAR-T的研究报告如雨后春笋、大大增加,同时,中国企业的身影也前所未有地活跃其中。
易慕峰生物正是这批参加ASGCT的中国企业之一,其创始人、董事长兼CEO孙敏敏提到,今年5月,易慕峰体内CAR-T技术平台亮相ASGCT后,受到广泛关注。
随着巨头竞逐、资本涌动、创新力量集结,这场以“体内编程”为核心的细胞治疗范式革命,正凭借其重塑治疗边界的磅礴潜力,以纵横捭阖之势,站在爆发的临界点。
TONACEA
细胞治疗“药物化”演变
体内CAR-T之所以被视为一种颠覆性前沿技术,源于其直指现有CAR-T(ex vivo CAR-T)的“阿喀琉斯之踵”。
加上7月30日获批的恒润达生“雷尼基奥仑赛注射液”,全球目前已上市的14款CAR-T疗法,无一例外属于体外制造。
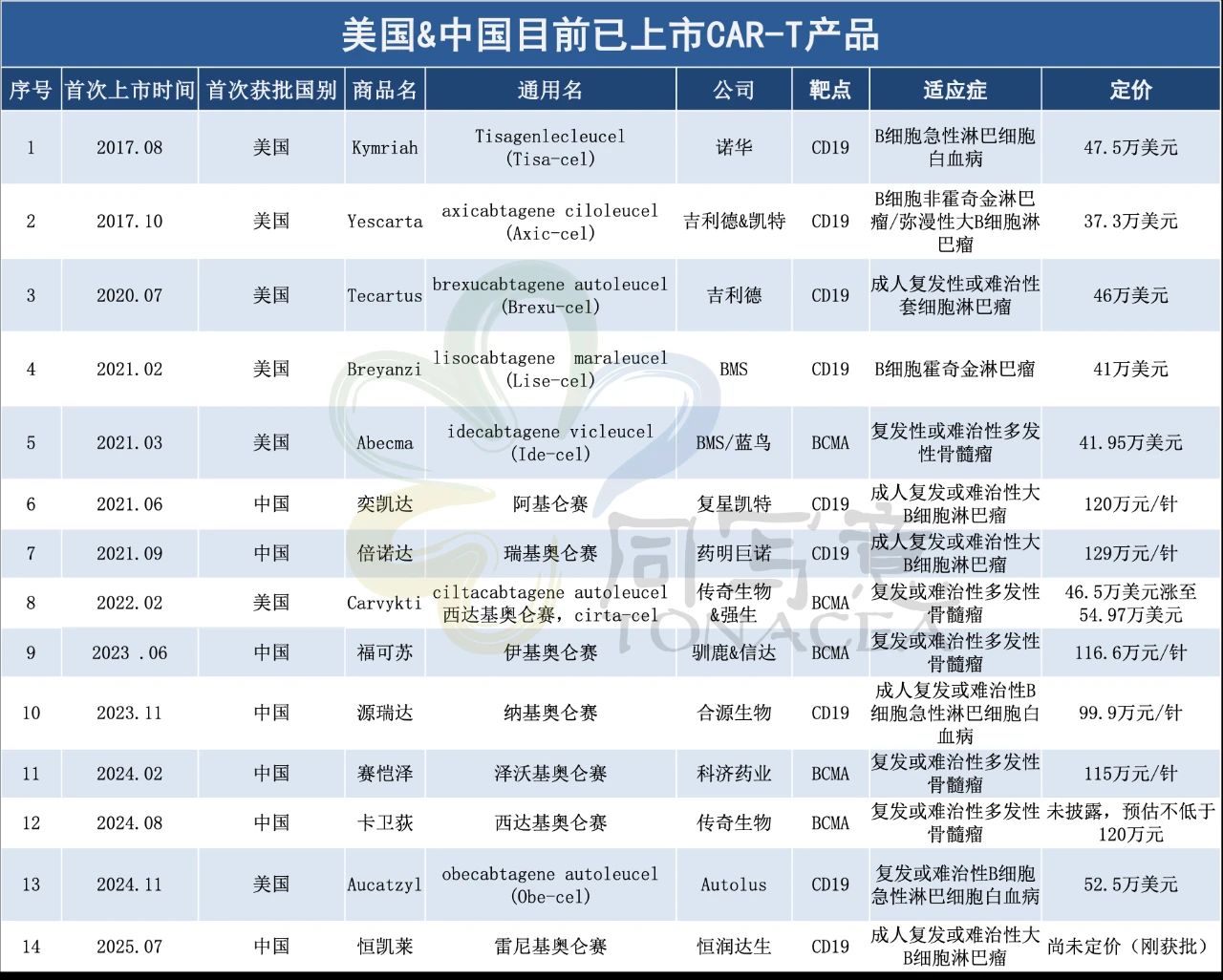
注:西达基奥仑赛于2022年2月在美国获批上市,并于2024年8月在中国获批上市。
它们虽然在肿瘤治疗效果上取得颠覆性突破,但其整体生产过程复杂、周期漫长且成本昂贵,无形中筑起了商业化和患者可及性的高墙。
具体来说,体外CAR-T需要医生从患者血液中提取T细胞,将其寄给制药公司,其技术人员使用慢病毒载体在这些T细胞表面递送并嵌入嵌合抗原受体(CAR),从而构建出CAR-T细胞,再将这些CAR-T细胞培养扩增到数亿个,然后冷冻保存、送回医院,最后输注到患者体内。
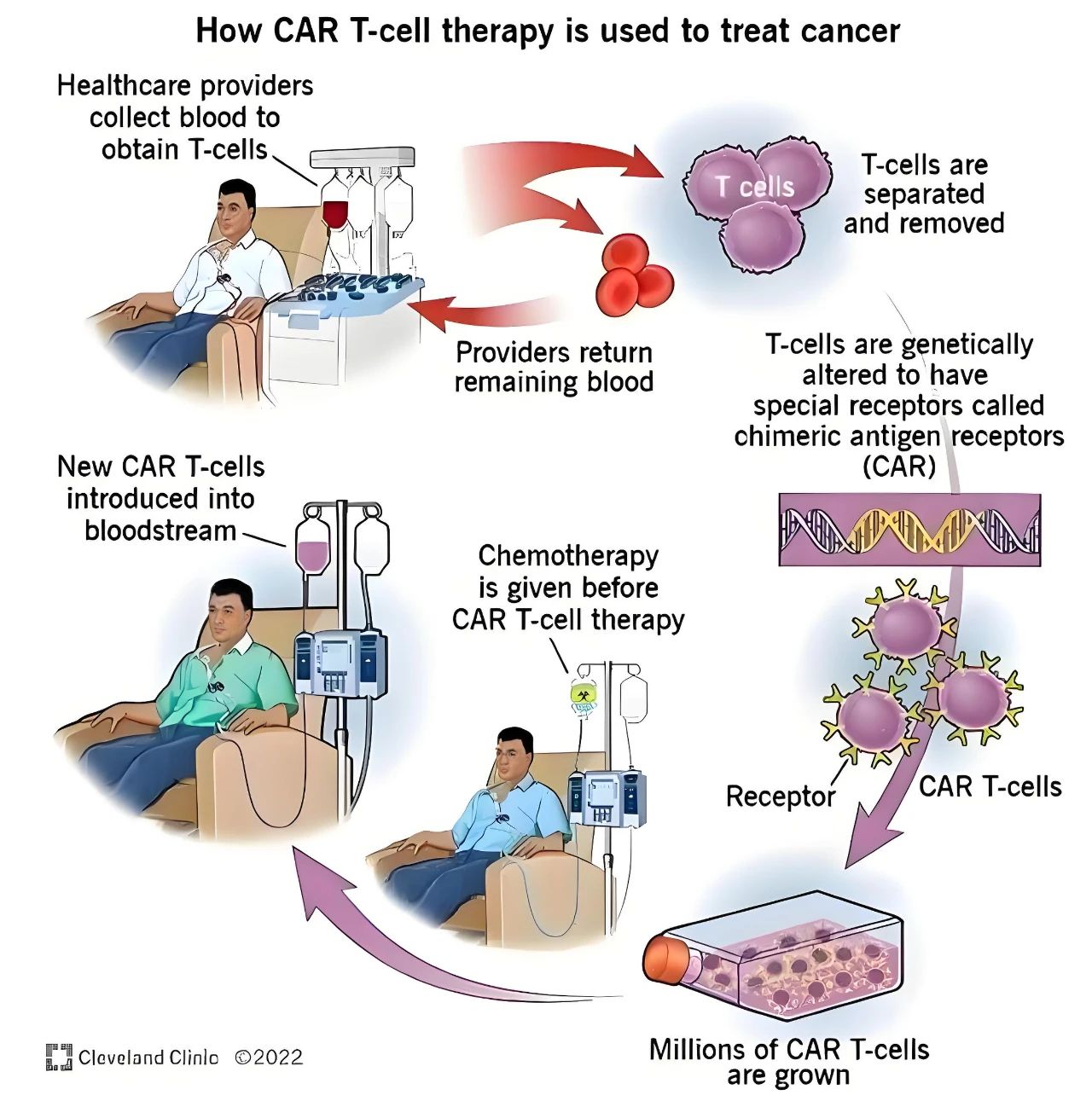
CAR-T产品治疗简介,来源:克利夫兰诊所
繁琐的过程,以至于在医疗发达的美国,也只有大约200家医疗中心能够给患者提供这种疗法。
同时,对于需求端的患者而言,化疗药物几乎可以立刻拿到,而CAR-T细胞疗法通常需要数周等待,再加上动辄数十万美元的高昂费用,患者在接受治疗前还需要先进行化疗清髓,这意味着许多本可受益于CAR-T细胞疗法的人最终未能接受治疗。
目前,在美国只有约20%的符合条件的患者成功接受了自体CAR-T治疗;而在中国,只有不到2%的符合条件的患者成功接受了自体CAR-T治疗。
因此,整个医疗界的深切呼唤是:CAR-T,能否更像一粒“药”?体内CAR-T,正是这终极答案的曙光。
合源生物CEO吕璐璐描绘了清晰的进化路径:CAR-T正经历从1.0代“个人定制” -1.5代“快速制备” -2.0代“通用型”(有限规模化)-3.0代“体内现货型” 的跃迁,逐步解决“可及性”的破壁。

来源:合源生物CEO吕璐璐
博生吉医药CEO杨林,则更直指核心:对比体外CAR-T的重重挑战,体内CAR-T真正实现了将复杂的细胞治疗技术转化为标准化药品的梦想。
TONACEA
更具可塑性的CAR-T
体内CAR-T疗法通过病毒载体、纳米载体等递送系统,把CAR基因直接递送到患者体内的T细胞中,实现在体内进行基因改造,省去了体外基因改造和扩增步骤。
云顶新耀CEO罗永庆在采访中指出,体内CAR-T因其off-shelf的通用型生产方式,且无需淋巴细胞清除化疗,为CAR-T的大规模临床应用提供可能性。
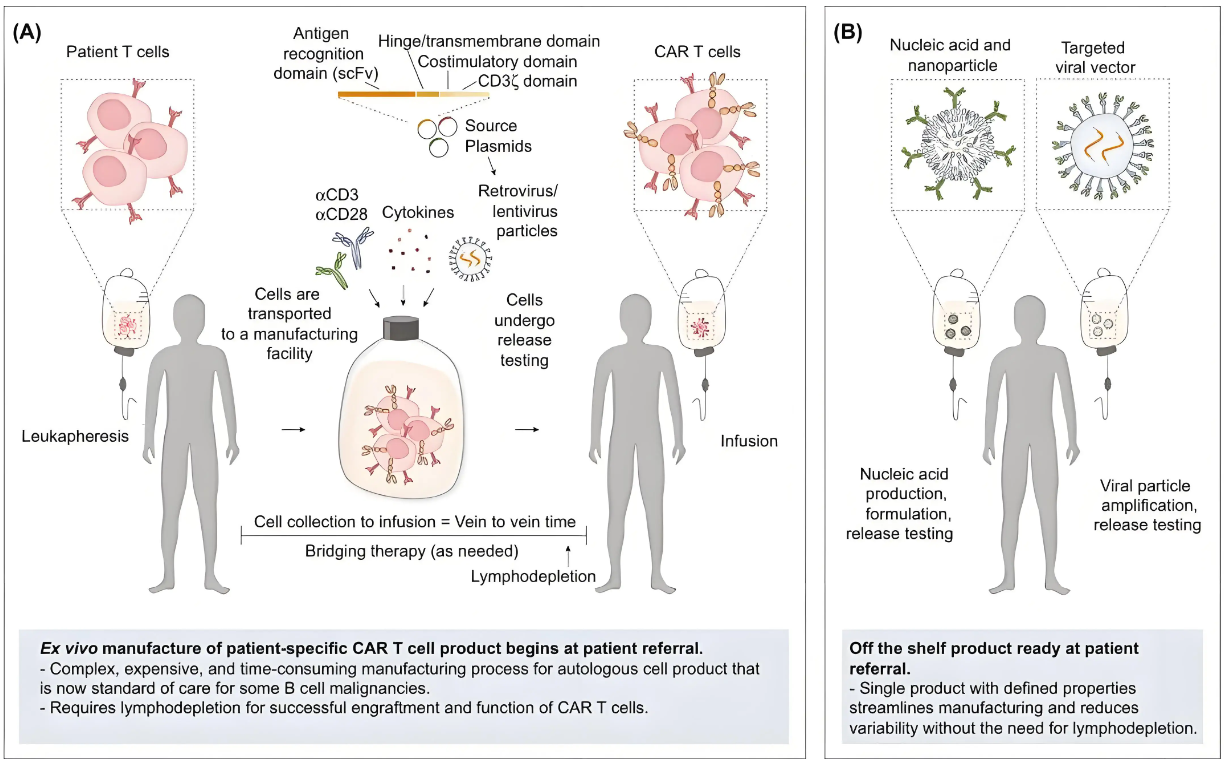
DOI: 10.1016/j.tips.2024.03.004
而且,这种“现货型”特征,大大简化了生产及治疗流程,有望显著降低治疗成本;同时,“现货”也有望满足更多急重症患者的临床需求,避免因病情恶化而错过治疗窗口。
杨林在演讲中也提到,通过一个病毒载体或者非病毒载体直接在体内生成CAR-T,不需要清淋处理——任何细胞治疗不需要清淋处理,本身就是一个很强的产品的竞争力。
从疗效来看,由于体内CAR-T疗法是在患者体内直接进行基因改造,能更好地模拟体内的生理环境,让改造后的T细胞能更好地适应并攻击肿瘤细胞。
这不仅能避免体外生产过程中可能出现的细胞污染和变异风险,患者也不需要接受化疗方案清除淋巴细胞,保持完整的免疫系统,避免化疗相关的副作用,如更大的感染风险。
现有临床前数据显示,体内CAR-T疗法不仅能够快速深度清除外周血及淋巴组织中的B细胞,并且,治疗后B细胞恢复以正常初始细胞为主,这能为免疫系统重置奠定基础。
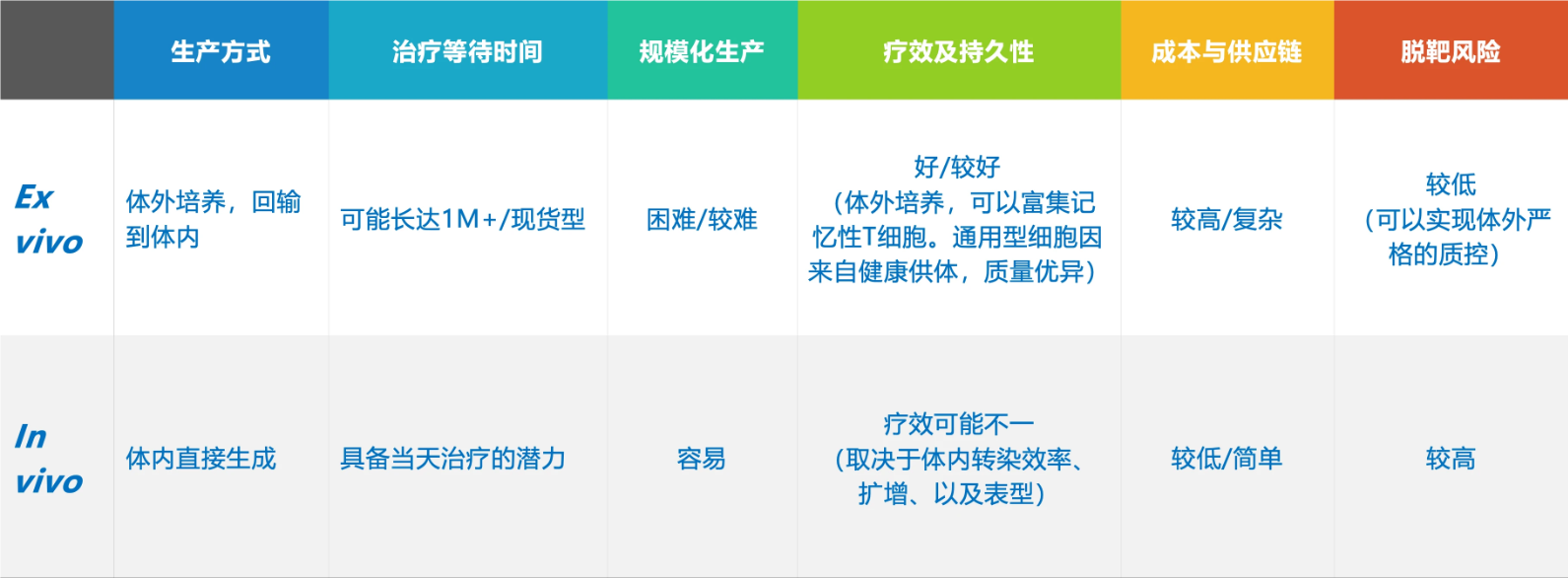
来源:博吉生医药CEO 杨林
应用范围的拓展是体内CAR-T的另一大亮点。
罗永庆指出,体内CAR-T不仅为肿瘤(包括血液瘤及实体瘤)提供新型的肿瘤免疫疗法,更为难治性的自身免疫等慢性疾病的治疗提供良好的治疗选择。
去年2月,德国埃尔朗根-纽伦堡大学的GeorgSchett教授团队,在NEJM杂志上报道了15例自免患者(8例系统红斑狼疮、4例系统性硬化症和3例特发性炎性肌病)在接受CAR-T疗法后重获新生。
艾伯维押注的Capstan,公司旗下CPTX2309就专注于B细胞介导的自身免疫疾病,如狼疮和多发性硬化。
自免疾病的治疗核心在于清除致病性B细胞并重建免疫耐受,理论上,体内CAR-T疗法能够通过瞬时或可控的CAR表达,为自免疾病提供高效且安全的解决方案。
TONACEA
技术路线之争
实现体内CAR递送面临严苛要求:必须精确靶向T细胞、实现高效基因转导并确保低毒性。这决定了体内CAR-T领域的角逐,本质上是递送技术的军备竞赛。
目前,体内CAR-T的主流技术策略分为两条:一个是基于慢病毒的技术体系,另一个是基于脂质纳米颗粒(LNP)的递送系统。
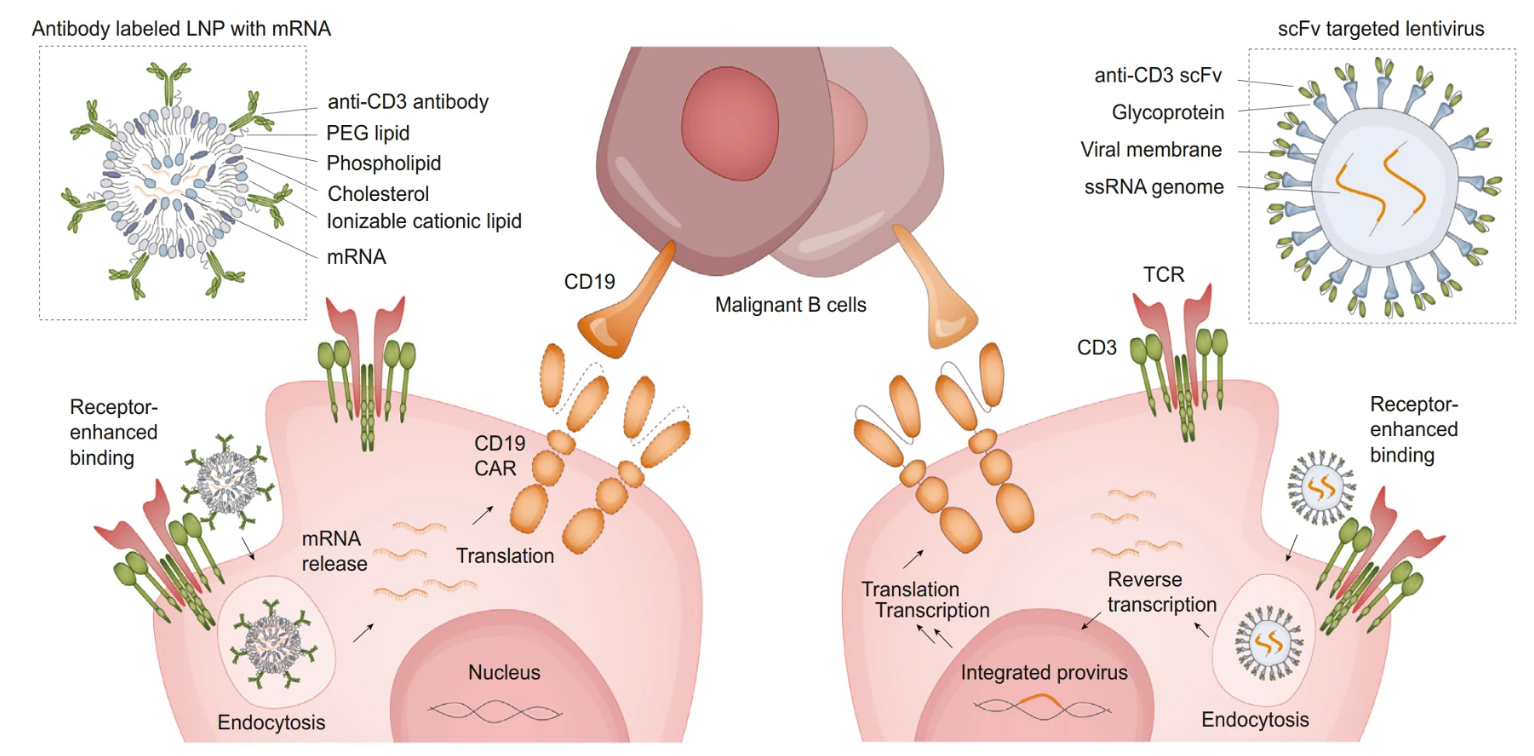
Short, Lauralie, et al. Trends in Pharmacological Sciences (2024).
前者是利用经过改造的、能够特异性感染T细胞的慢病毒载体递送CAR基因;后者则是利用LNP包裹mRNA或DNA,并通过特定配体靶向递送至T细胞。
其中,慢病毒载体由于发展时间较久,并在已获批的传统CAR-T疗法中积累了较多CMC以及临床经验,进度较快。
目前第一梯队的几家国外公司(Interius、Umoja、EsoBiotec),均是慢病毒体系的玩家,已产生3个处于临床I期的产品,并与MNC达成了4个big deal。
孙敏敏指出:慢病毒载体的特点就是稳定转导,疗效与传统CAR-T相似,安全性上可能存在基于病毒的免疫毒性和插入的风险,为此易慕峰也针对性做了策略去减缓毒性,在成本上,随着慢病毒生产体系的“内卷”以及不断升级,预期成本可以降到数千元/剂。
当然,使用慢病毒载体也存在挑战。
目前大多数基于慢病毒体系的公司采用的是传统VSV-G的慢病毒,VSV-G具有泛嗜性,结合LDLR会引起正常细胞的泛感染。通过突变,VSV-G可以避免与正常细胞结合,但也影响了转导T细胞的功能,多数的VSV-G突变体有专利风险。
针对T细胞嗜性和激活,通过整合新型T细胞靶向模块,可以使慢病毒转导T细胞的功能恢复。如果没有激活,T细胞的效应功能比较弱。
此外,在慢病毒的稳定性方面,病毒颗粒容易被巨噬细胞吞噬,VSV-G假型的慢病毒载体更容易被中和抗体IgG、IgM和补体功能失活。
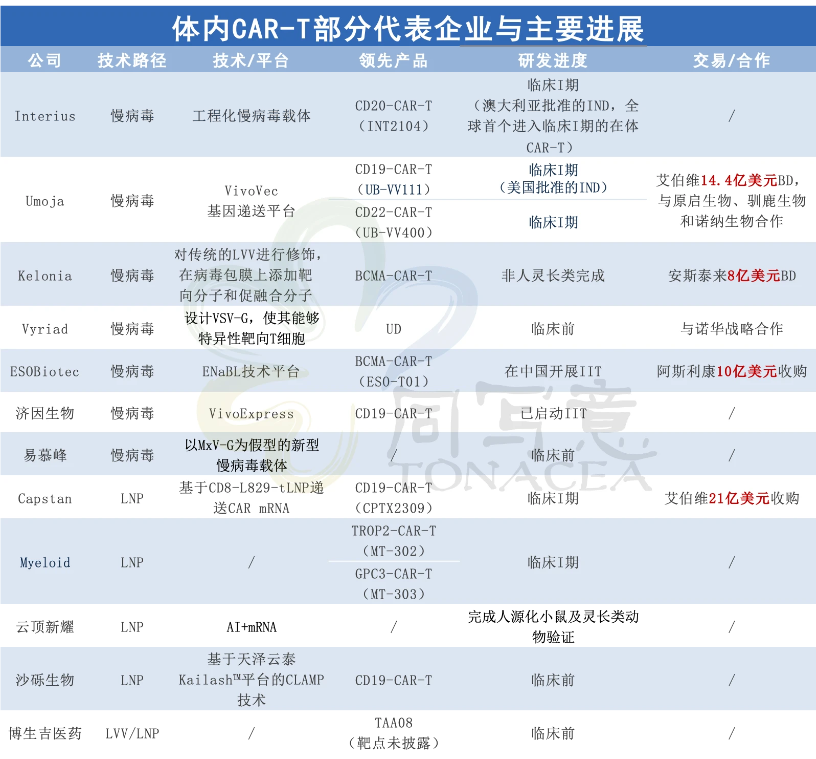
慢病毒路线之外,当下,基于LNP载体的体内CAR-T正加速发展,很多新入局这一赛道的公司普遍采用这一路线。
“最容易看到的第一印象是,慢病毒存在基因整合的风险,LNP最大的一个优势在于非基因整合风险。”杨林说道。
杨林粗略统计了2025ASGCT年会的部分摘要,其中一半都是基于LNP路线(10篇),5篇慢病毒、2篇纳米颗粒、1篇AAV,“说明大家都在采用不同的strategy尝试,但LNP多是不是就意味着LNP更有远景的?这需要客观来看”。
罗永庆直指技术核心:以mRNA平台为例,抗体耦联LNP的能力,T细胞的转染效率,AI赋能的mRNA序列设计,LNP的主动靶向递送能力,CMC放大优化都很重要。前期对产品的掌控力高,拥有全平台端到端的能力能极大地优化有效性与安全性,缩短开发时间,提高开发效率。
现阶段,LNP领域跑得最快的,以Capstan为代表之一,其抗CD19体内CAR-T细胞疗法CPTX2309已于6月正式开始I期临床试验,用于治疗B细胞介导的自身免疫疾病。
根据公司发表的论文,临床前实验结果显示,在啮齿类动物模型(人源化小鼠)和非人灵长类动物模型(食蟹猴)中,该公司专有的靶向脂质纳米颗粒(tLNP)成功将CAR mRNA靶向递送到体内的CD8+T细胞,显示出对癌症和自身免疫疾病良好的治疗前景和安全性。
不过,杨林在现场也指出,要客观看待里面可能出现的问题,“它3剂量的给药,毒副作用明显高于2剂量的,也就是说,在小鼠实验中,存在剂量依赖,这是我们不太希望看到的现象”。
总结来看,Capstan最大的优势在于解决了肝靶向问题,显著降低肝脏脱靶递送,提升脾脏及T细胞特异性递送效率,“所有进行LNP路线的玩家第一步都要解决这个问题”。其次,CD8抗体靶向设计实现CD8+ T细胞选择性工程化,减少CD4+ T细胞激活相关风险。
不过,仍有很多问题仍需进一步优化,例如,多次给药面临免疫原性的挑战;对于需要维持长期药效持续性的适应症(例如肿瘤等),存在巨大挑战。

来源:博生吉医药CEO杨林
两条技术路线各有优劣势,杨林现场作了一个恰如其分的比喻,“LNP可能是先甜后苦,很多问题还没暴露,慢病毒可能是先苦后甜,一开始改造时很多挑战,但后续它的CMC体系非常成熟,临床上暴露的问题也很充分”。
TONACEA
MNC巨头跑步进场
MNC的布局,向来是行业发展的风向标。在体内CAR-T这片前沿热土,巨头们已悉数下场,以多元方式全力“卡位”。
艾伯维先是以14.4亿美元携手Umoja,6月更以21亿美元现金“豪娶”Capstan,将体内CAR-T的两大技术路线尽收囊中。
阿斯利康同样大手笔。5月,阿斯利康正式完成对EsoBiotec的收购,这笔交易总价值高达10亿美元,收购完成后,阿斯利康获得了其核心的工程纳米抗体慢病毒(ENaBL)平台及4条在研管线。
EsoBiotec是一家进展较快的in-vivo细胞疗法企业,开发了核心技术平台ENaBL,能够通过高度靶向性慢病毒载体向特定免疫细胞(如T细胞)递送目的基因,且支持简单的静脉注射给药无需免疫细胞耗竭,极大地简化了治疗流程。
赛诺菲在2023年披露公司有三个体内CAR-T项目处于临床前开发阶段;安斯泰来在去年2月宣布与Kelonia达成合作以开发体内CAR-T,潜在交易总额超8.75亿美元;诺华也于同年11月,与Vyriad达成了开发体内CAR-T的战略合作。
除了摆在明面上的合作与收购,细翻赛道内明星公司的投资者,也能发现MNC的身影。
如今年刚走出“隐身模式”的Stylus Medicine,基于重组酶的新型基因编辑技术开发体内CAR-T,其8500万美元首轮融资的参投者包含了礼来、强生、RA Capital等知名机构。
至于艾伯维刚收入囊中的Capstan,创始团队成员集齐了“CAR-T之父”Carl June、“mRNA技术奠基人”Drew Weissman、“体内原位 CAR-T 技术发明人”Jonathan Epstein,堪称“天团阵容”。
“天团下场,巨头追逐”,早期Capstan1.65亿美元的种子和A轮融资,来源于诺华、辉瑞、拜耳、礼来、BMS等的投资。
收购、合作、投资——巨头正编织起一张多维的网,誓要在这重塑细胞治疗格局的“战略要塞”上,插上自己的旗帜。
TONACEA
破晓前的寂静与脉动
纵观全局,体内CAR-T需求潜力如海,创新热情似火,然而,绝大多数管线仍处于临床前阶段,临床数据的星光尚显稀疏。
一切仍有待临床的庄严验证。
趋势如灯塔,方向已昭然。就像吕璐璐所言,“趋势和方向都是明确的,就看各家通过怎样的技术平台,真正去把它干出产品,解决一部分患者的痛点。”
罗永庆也指出:如何能顺利从临床前转向临床开发,提高开发效率就成为关键,这些与产品和技术平台有很大关系。
答案或许尚未完全显现,但一场细胞治疗领域的深刻嬗变,已然在寂静中积蓄着力量。
整体来看,体内CAR-T作为真正有望实现细胞治疗的“药物化”的前沿领域,是创新药发展的重要趋势和风口,代表着细胞治疗未来的战略方向,并将成为重塑行业格局的关键高地。
纵然技术尚在破晓前的幽谷穿行,前路挑战如嶙峋山石,但近年间骤然加速的脉动与蓄积的能量,已如地平线上渐染的金边,昭示着:这不再是一场纸上谈兵,而是一场即将喷薄而出的黎明。
体内CAR-T风口已至,细胞治疗“弯道超车”的历史性机遇就在眼前!
9月17-18日,同写意将联合益诺思、清大浦安、基锘威生物等机构,在上海举办“未来细胞疗法决策者峰会暨体内CAR-T开拓者研讨会”,通过技术研讨、资本推动、供应链/CRO赋能,审评指导与临床验证的闭环联动,让前沿科技快速度转化为普惠性的治疗方案。
上一页
相关新闻





